Das Atom

- Atomtheorie
- Allgemeine Gesetze
- Elementarteilchen
Inhaltsübersicht
Elemente bestehen aus Atomen, welche zu den kleinsten Teilchen gehören. Der Begriff Atom leitet sich aus dem griechischen Wort „atomos“ ab und bedeutet „unteilbar“. Durch die moderne Technik lassen sich Atome heute mit dem bloßen Auge „erkennen“. Hierfür werden bestimmte Mikroskope, wie Transmissions- oder einfache Elektronenmikroskope, verwendet.
John Dalton und seine Atomtheorie
John Dalton war ein bedeutender englischer Naturwissenschaftler und formulierte aus seinen eigenen Beobachtungen seiner chemischen Experimente einige Aussagen, die bis heute ihre Verwendung finden. Somit stellte er das erste wissenschaftlich fundierte Atommodell auf (1803-1808), welches sich in vier Kernaussagen unterteilen lässt:
- Elemente bestehen aus Atomen, also aus extrem kleinen Teilchen.
- In einem Element sind nur gleiche Atome vorzufinden, aber die Atome unterschiedlicher Elemente sind verschieden.
- Bei chemischen Reaktionen werden Atome miteinander verbunden oder voneinander getrennt, aber niemals zerstört oder erzeugt. Atome eines Elements werden also nicht in das eines anderen Elements umgewandelt.
- Eine chemische Verbindung resultiert aus der Verknüpfung von Atomen aus zwei oder mehr Elementen. Eine Verbindung besteht immer aus den gleichen Atomsorten, die in bestimmten Anzahlverhältnissen miteinander verknüpft sind.
Diese vier Hauptaussagen können in den drei folgenden Gesetzen formuliert werden:
Allgemeine Gesetze
Erstes Gesetz
Das erste Gesetz ist das Gesetz von der Erhaltung der Masse (von Dalton). Es sagt aus, dass während einer chemischen Reaktion keine Veränderung der Gesamtmasse zu beobachten ist.
m (Edukte) = m (Produkte)
Verbrennt man zum Beispiel Stahlwolle - bestehend aus Eisen - an der Luft, so nimmt das Gewicht zwar zu, allerdings wird bei der Verbrennung Sauerstoff aus der Luft gebunden. Somit lässt sich folgende Summenformel aufstellen: 4 Fe (s) + 3 O2 (g) → 2 Fe2O3 (s). Dabei steht s für “fest” (engl. solid) und g für “gasförmig”.
In der Summenformel wird die Anzahl der einzelnen Atome in einem Molekül (einer Substanz) als tiefgestellte Zahl nach dem Elementsymbol angegeben.
Zweites Gesetz
Das zweite Gesetz ist das Gesetz der konstanten Proportionen (von Proust, 1799) und beschreibt das Massenverhältnis. Es besagt, dass in einer Verbindung stets dieselben Elemente im gleichen Massenverhältnis enthalten sind.
m (Element x) / m (Element y) = const.
In 1 g H2O sind 0,889 g Sauerstoff und 0,111 g Wasserstoff enthalten. Das Massenverhältnis von Sauerstoff zu Wasserstoff ist 8 zu 1. In 50 g H2O sind 44,44g Sauerstoff und 5,56 g Wasserstoff enthalten und auch hier beträgt das Verhältnis von Sauerstoff zu Wasserstoff 8 zu 1. Wir sehen also, dass bei einer Verbindung stets die gleichen Elemente im gleichen Massenverhältnis enthalten sind.
Drittes Gesetz
Das dritte und somit letzte Gesetz ist das Gesetz der multiplen Proportionen (von Dalton). Auch hier geht es wieder um die Verhältnisse, allerdings um die von mehreren Verbindungen. Denn wenn zwei Elemente, A und B, mehr als eine Verbindung eingehen, so steht die Masse von A, die sich mit einer bestimmten Masse von B verbindet, in einem ganzzahligen Verhältnis zueinander.
Zum Beispiel können Sauerstoff und Wasserstoff nicht nur Wasser bilden, sondern auch Wasserstoffperoxid. Bei H2O wissen wir bereits, dass das Massenverhältnis immer 8:1 ist. Allerdings ändert sich das bei Wasserstoffperoxid, H2O2, denn hier liegt das Verhältnis von Sauerstoff zu Wasserstoff bei 16:1.
Während einer Elektrolyse kann Wasser durch Anlegen einer elektrischen Spannung in seine Bestandteile zerlegt werden. Da sich doppelt so viel Wasserstoff wie Sauerstoff bildet und unter der Annahme, dass gleiche Mengen eines Gases das gleiche Volumen einnehmen, liegt das Verhältnis H:O = 2:1 vor. Demnach wird bestätigt, dass es sich um Wasser handelt.
Elementarteilchen
So wie die meisten Modelle wurde auch die Atomtheorie von Dalton verbessert. Denn nach Dalton’s Theorie waren die Atome die kleinsten unteilbaren Teilchen. Allerdings stellte man gegen Ende des 19. Jahrhunderts fest, dass es noch kleinere gibt. Die Atome selbst bestehen aus noch viel kleineren Teilchen und werden als Elementarteilchen bezeichnet.
Diese setzen sich aus drei Teilchen zusammen: Neutron, Proton und Elektron. Ein Atom stellt man sich so vor, dass es aus einem Kern besteht und eine umliegende Hülle besitzt. Der Atomkern setzt sich aus den Nukleonen, den Neutronen und Protonen zusammen, während die Hülle die Elektronen enthält. Das Proton ist positiv und das Elektron negativ geladen. Das Neutron hingegen besitzt keine Ladung.
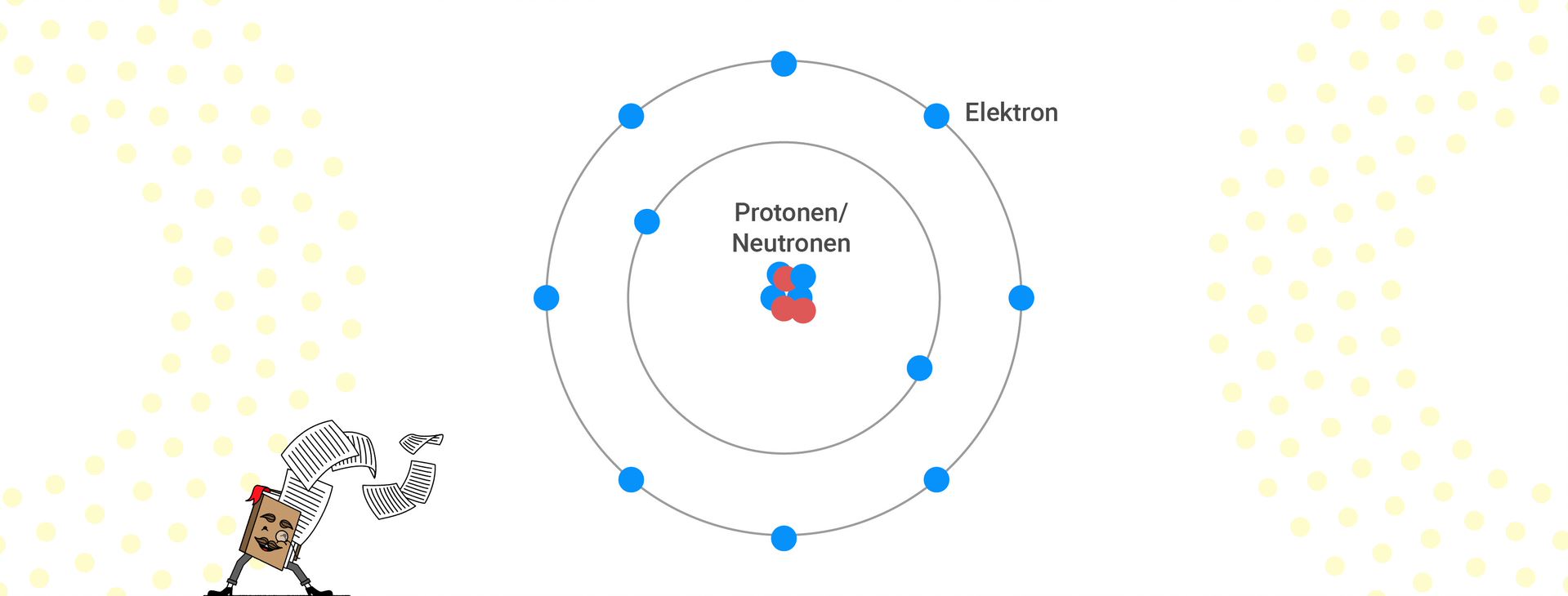
Die Ladung des Elektrons qe = -e (Elementarladung) beträgt -1,6022∙10-19 C und somit gilt auch für die Ladung des Protons qp = +e ein Wert von +1,6022∙10-19 C. Da das Neutron neutral ist, ist die Ladung qn = 0. Die Masse des Protons mp und des Neutrons mn betragen 1,6749∙10-27 kg. Da das Elektron viel kleiner ist, beträgt die Masse des Elektrons me nur 9,1094∙10-31 kg. Diese absoluten Massen werden aufgrund ihrer sehr kleinen Zahlenwerte kaum verwendet, stattdessen benutzt man die atomare Masseneinheit u (Dalton). Dabei entspricht 1 u etwa so viel wie 1,6606∙10-27 kg.
Da ein Atom aus den drei Elementarteilchen besteht, lässt sich die Masse eines Atoms einfach herleiten. Die Masse eines Elektrons ist allerdings so gering, dass hauptsächlich Protonen und Neutronen die Masse des Atoms bestimmen und die Masse der Elektronen vernachlässigt werden kann. Einfachheitshalber werden die Massen für Proton und Neutron als 1 u angenommen und für Elektronen 0.
In einigen Periodensystemen werden Angaben zu den Atomen gemacht. Die Massenzahl A bzw. Atommasse, angegeben in u, gibt die Anzahl der Nukleonen wieder (A = Np + Nn). Aus der Ordnungszahl Z lässt sich die Anzahl der Protonen, also positiven Elementarladungen, im Kern herrauslesen (Z = Np). Jedes Element hat eine eigene Ordnungszahl. Somit lässt sich die Anzahl der Neutronen aus der Differenz der Massenzahl und der Ordnungszahl herausfinden. Im Atom ist die Anzahl der Protonen Np gleich der Anzahl der Elektronen Ne, damit die Gesamtladung 0 beträgt. Somit stellt die Ordnungszahl ebenfalls die Anzahl der Elektronen dar. Sollten mehr Protonen als Elektronen vorzufinden sein, so handelt es sich um ein positiv geladenes Ion, genauer Kation. Bei einer Anwesenheit von mehr Elektronen spricht man von einem Anion, ein negativ geladenes Ion. Im Periodensystem sind nur neutral geladene Elemente zu finden, um Ionen zu erhalten, muss daher eine chemische Reaktion ablaufen.
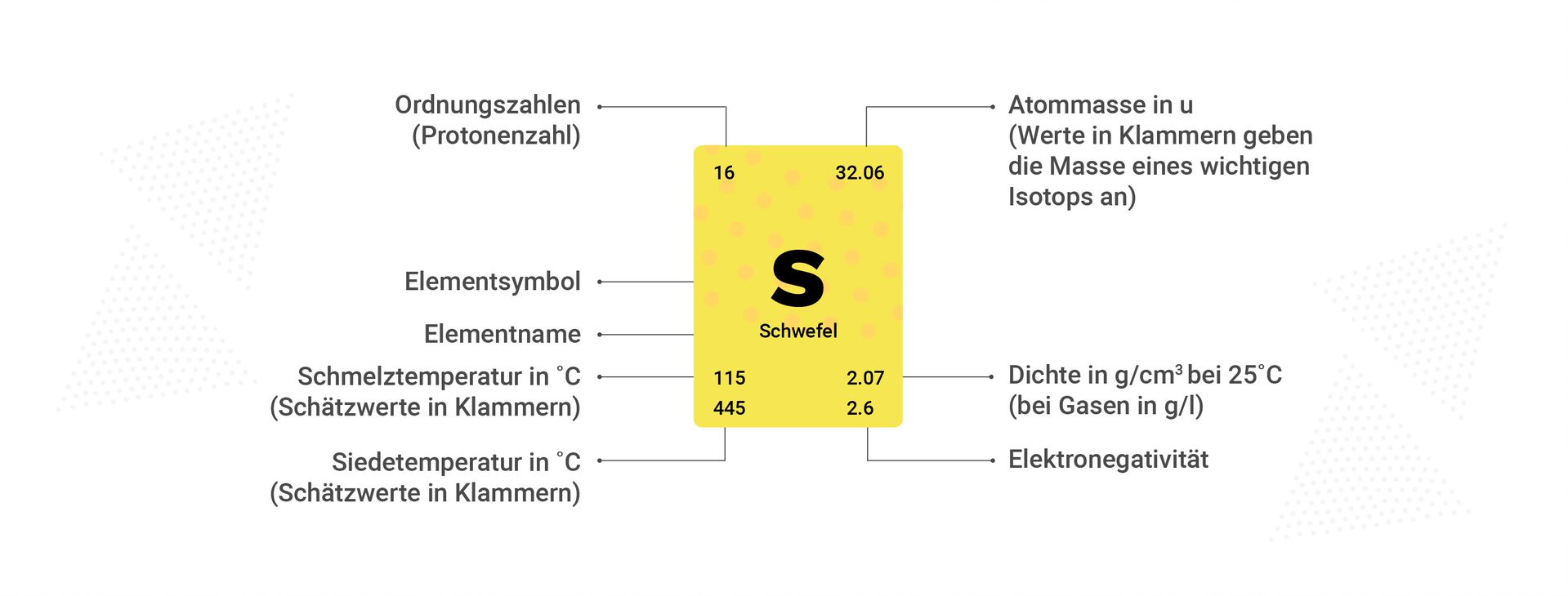
Falls du dich wunderst, warum die Atommasse einiger Elemente Nachkommastellen besitzt, so denke daran, dass die Massen der Protonen und Neutronen nicht wirklich 1 u wiegen, sondern etwas mehr und die Elektronen zudem eine geringe Masse besitzen.
Du suchst hilfreiche Dokumente zum Thema?
Auf Studydrive findest du jede Menge Lernmaterialien, die dir bei der Kurs- oder Prüfungsvorbereitung helfen werden. Hier findest du Zusammenfassungen und Notizen, Lösungen zu vergangenen Prüfungen und Arbeitsblätter.


