Die besten Zusammenfassungen zum Thema Thermodynamik

Thermodynamik_Crashkurs.pdf

Thermodynamik_wichtige_Formeln.pdf

Thermodynamik_Zusammenfassung.pdf

Thermodynamik_Zusammenfassung.pdf

Thermodynamik_1_Zusammenfassung.pdf


Das Modul „Thermodynamik“ gehört zu den Grundlagenmodulen des Maschinenbaus, der Verfahrenstechnik und der Energietechnik. Mit Thermodynamik verbindet man häufig auch die sogenannte Wärmelehre, welche ihren Ursprung im Studium der Dampfmaschinen hat. In der Vergangenheit hat man versucht, die Umwandlung von Wärme in mechanische Arbeit zu studieren (N.L.S. Carnot). Heute liefert die gesamte Thermodynamik die Grundlagen für die Strömungsmechanik sowie für die Wärmeübertragung. Deshalb gilt die Thermodynamik unter anderem auch als eine eigene natur- und ingenieurwissenschaftliche Disziplin.
Da viele ingenieurswissenschaftliche Studiengänge die Thermodynamik im Studienplan eingebunden haben und das Modul für die meisten Studierenden eher komplex und nicht direkt durchsichtig erscheint, ist es umso wichtiger die technischen Vorgänge und Prinzipien zu verstehen, um schlussendlich das Modul auch zu bestehen zu können, da in der Klausur definitiv Transferwissen abgefragt wird.
In der Thermodynamik von heute beschäftigt man sich nicht nur mit der Wärmelehre, sondern auch mit der allgemeinen Energielehre. Ziele dabei sind::
Häufig treten in vielen technischen Anwendungen beide Zielsetzungen auf. Verstärkt befasst sich die Thermodynamik auch mit Prozessen, wenn an den Prozessen Wärme beteiligt ist, ohne detailliert verschiedene Stoffe zu analysieren. Kreisprozesse (Zustandsänderungen eines Arbeitsmediums) kommen häufig vor und andererseits trifft die Thermodynamik, wie bereits erwähnt, Aussagen über Stoffe wie die verschiedenen Aggregatzustände und ihren Wechsel (Siedetemperatur, Schmelztemperatur, Verdampfungstemperatur…).
In den Kreisen der Naturwissenschaften ist die Thermodynamik sehr bedeutsam. Der Grund dafür ist, dass bei allen in der Natur stattfindenden Prozessen auch eine Energie beteiligt ist. Sie bietet Einblick in die Eigenschaften der Materien sowie eine Verbindung zu anderen Ingenieursbereichen wie die klassische Mechanik oder der Quantenmechanik.
In der Ingenieurwissenschaften nutzt man die Thermodynamik auch für Analyse, Berechnung und Konstruktion von zahlreichen Maschinen oder Anlagen, wie z.B. Wärmekraftmaschinen (Dampfmaschine, Dieselmotor, Gasturbine), Arbeitsmaschinen (Pumpen, Verdichter), Klima- und Kältetechnik, Wärme- und Stoffübertragung, Energietechnik (Kraftwerke)
Eine große Bedeutung in der Thermodynamik haben die zwei Hauptsätze:
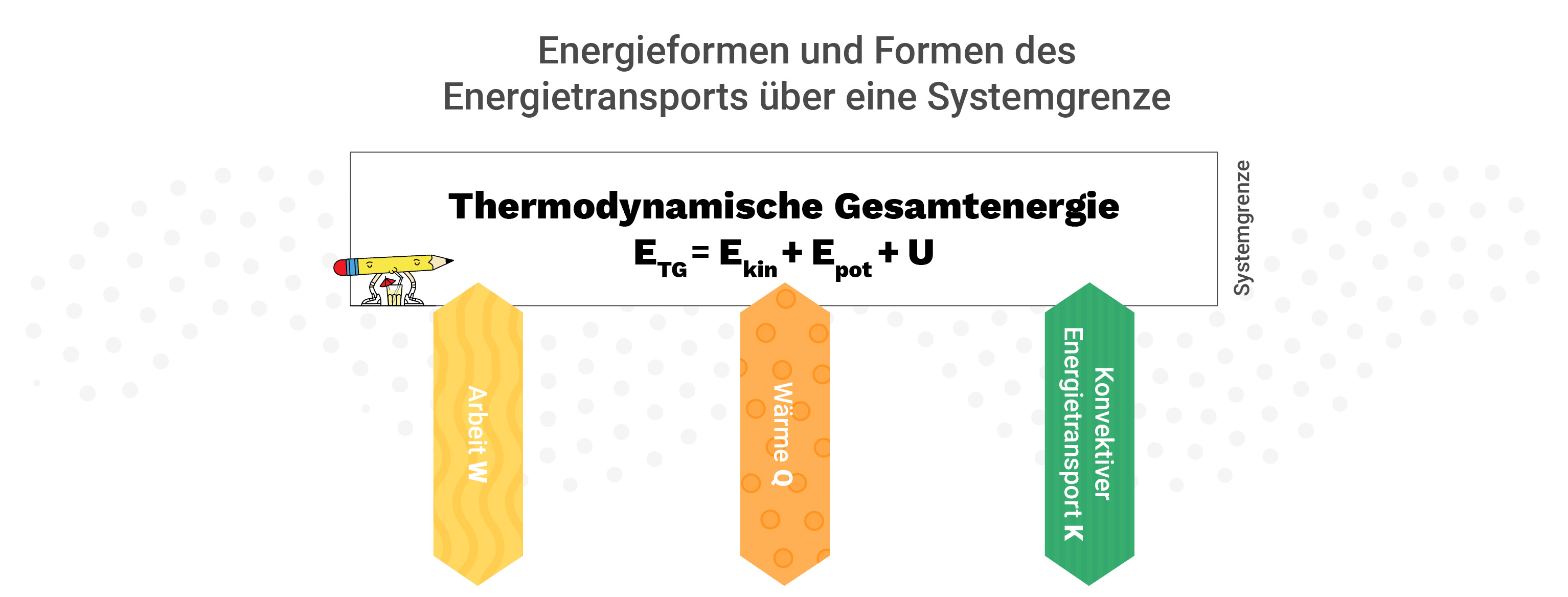
Hauptsatz: E=Konst. Mit der Gesamtenergie E. Der erste Hauptsatz besagt, dass die Gesamtenergie E in einem abgeschlossenen System konstant ist. Die Energie kann lediglich von einer Form in die andere geändert werden. Energie kann weder geschaffen noch zerstört werden. In der gesamten Physik hat sie als Energieerhaltung ihre Gültigkeit!
Hauptsatz: Sirr ≥ 0 Mit der Entropieproduktion Sirr. Der zweite Hauptsatz sagt aus, in welcher Richtung Energieumwandlungen möglich sind. Die thermische Energie ist bekanntlich nicht in beliebigen Maßen umwandelbar. Als Beispiel können mechanische, elektrische oder chemische Energie gänzlich in Wärmeenergie umgewandelt werden. Im Gegensatz dazu lässt sich Wärmeenergie nur teilweise und nur mit sehr hohem technischen Aufwand in andere Energie umwandeln.
Die zwei Hauptsätze sehen auf dem ersten Blick trivial aus, aber die Herausforderung, die hier besteht, ist das Verstehen der physikalischen Vorgänge der Probleme sowie das Abstrahieren der Probleme und besonders komplexe physikalische Modelle zu erstellen, in denen wichtige Einflussgrößen miteigebunden werden sollten.
Folgende physikalische Größen sind geeignet, um den thermodynamischen Zustand eines Systems zu beschreiben.
Energie von der Materie wird in verschiedenen Zuständen (fest, flüssig, gasförmig, magnetisiert, etc.) beschrieben. Dabei wird die Materie oft als isotrop, also das Aufweisen der gleichen physikalischen und chemischen Eigenschaften nach allen Richtungen hin, angesehen. Daher kann anstelle der üblichen Ortsvariablen x, y, z nun das Volumen „V“ als Variable verwendet werden. Das spezifische Volumen „v“ ist ebenfalls nicht unwichtig und wird als Quotient von Volumen und Masse definiert.
Spezifische Volumen: v= V/m
Der Druck einer Flüssigkeit, eines Gases oder eines isotropischen Festkörpers wird mittels Druckstempeln und einer Fläche A über die Kraft F gemessen.
P=F/A mit (p)= Pa=NM ^-2
Wenn zwei Körper im thermischen Gleichgewicht stehen, besitzen sie dieselbe Temperatur.
0. Hauptsatz:
Zwei Systeme, welche sich jeweils im thermischen Gleichgewicht mit einem dritten System befinden, stehen auch untereinander im thermischen Gleichgewicht. Die neue Zustandsgröße T existiert also, wenn ein thermodynamisches System (Gas, Flüssigkeit) im Gleichgewicht ist, welches dann eine definierte Temperatur hat.
Praxisbeispiel:
Temperaturausgleich: Entsteht, wenn man einen Körper (z.B. eine zu kühlende Wasserflasche) in eine kalte Umgebung aussetzt.
Konzentrationsausgleich: Zum Beispiel ein heliumgefüllter Luftballon, der diffusionsdurchlässig ist, welcher mit der umgebenden Luft in Verbindung gebracht wird.
Thermodynamische Zustandsgleichung
Beschreibt den mathematischen Zusammenhang zwischen den thermodynamischen Zustandsgrößen eines Systems. Dabei gilt: Der Zustand eines reinen Stoffs im flüssigen, festen oder gasförmigen Zustand kann generell durch zwei Zustandsgrößen eindeutig definiert werden. Die thermodynamische Zustandsgleichung wird gebraucht, um die Eigenschaften von Fluiden, Feststoffe oder auch Fluidgemischen beschreiben zu können.
Die thermische Zustandsgleichung verknüpft die drei Zustandsgrößen V, T, P miteinander über die Funktion p= p(v, T).
Die thermische Zustandsgleichung für ideale Gase lautet: p*V = m*Ri*T
Auf Studydrive findest du jede Menge Lernmaterialien, die dir bei der Kurs- oder Prüfungsvorbereitung helfen werden. Hier findest du Zusammenfassungen, Notizen, Lösungen zu vergangenen Prüfungen und Arbeitsblätter.











Mit unserem smarten Karteikarten-Tool kannst du dein Wissen schnell und effektiv testen oder easy von unterwegs lernen. Erstelle einfach deine eigenen Karteikarten oder übe mit denen deiner Kommilitonen.
Melde dich jetzt bei Studydrive an und erhalte kostenlos Zugang zu allen Kursen, die zu deinem Thema passen. Tausche dich außerdem mit anderen Studierenden aus und bekomme hilfreiche Antworten auf all deine Fragen!