Stoffgemische, Redoxreaktionen und Reaktionsgleichungen

Inhaltsübersicht
Stoffgemische
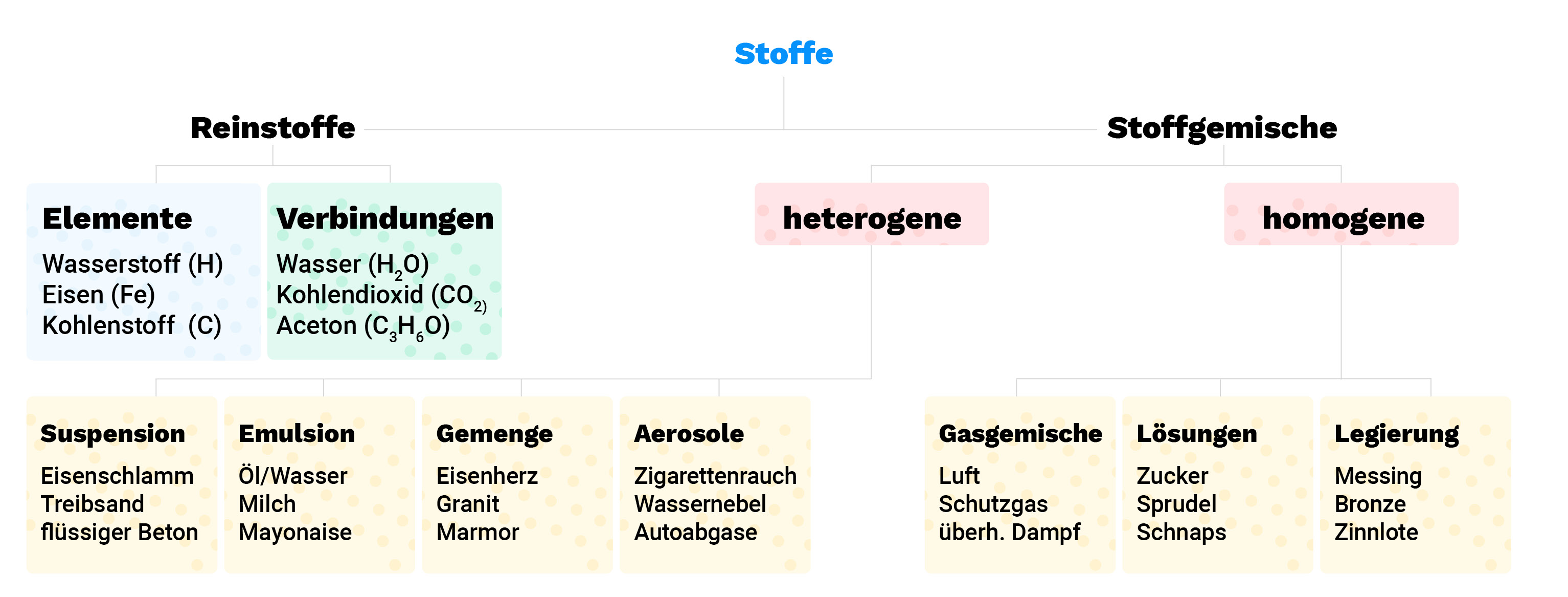
Stoffe kommen in der Natur eher selten als Reinstoffe vor. Es handelt sich dabei meistens um Stoffgemische, die aus mindestens zwei verschiedenen Reinstoffen zusammengesetzt sind. Selbst die hochreinen Chemikalien aus dem Labor beinhalten Verunreinigungen, auch wenn diese nur in geringem Maße enthalten sind. Stoffgemische kann man daher überall finden. Es gibt verschiedene Arten von Stoffgemischen, die ich im Folgenden erklären werde.
Heterogene Stoffgemische
Der Begriff “heterogen” kommt auch aus dem Griechischen und bedeutet verschiedenartig. Jedoch versteht man unter diesem Begriff in der Physik und in der Chemie, ein System oder ein Gemisch, e-welches mehrere Phasen umfasst. Bei einem heterogenen Stoffgemisch sind die Stoffe so miteinander vermischt, dass man die verschiedenen Bestandteile mit bloßem Auge voneinander unterscheiden kann. Zu beachten ist, dass die verschiedenen Bereiche im Stoffgemisch verschiedene Eigenschaften haben, wie beispielsweise unterschiedliche Farben, Aggregatzustände oder Härte.
Kolloidale Stoffgemische
Bei manchen Stoffgemischen sind die einzelnen Phasen oftmals makroskopisch nicht mehr so einfach zu unterscheiden. Sie sind fein zerteilt. In Fällen wie diesen spricht man von kolloidalen Systemen. Diese Systeme bestehen aus einer dispersen Phase, welche mehr oder weniger fein verteilt sind, und einem Dispersionsmittel. Zu erwähnen ist, dass die Kolloide auch netzartig miteinander verbunden sein können und, dass kolloidale Partikel oft keine einheitliche Größe besitzen.
Milch ist ein Phasengemisch aus einer wässrigen und einer fettartigen Phase, was erst unter dem Mikroskop zu erkennen ist. Streng genommen handelt es sich um eine Öl-in-Wasser-Emulsion. Dies bedeutet, dass einzelne Öltröpfchen vom Wasser umhüllt sind. Bei diesen Emulgatoren handelt es sich um Eiweiße. Sie weisen einen polaren und unpolaren Molekülteil auf. Die unpolaren Enden ragen in die Fett Tröpfchen hinein und die polaren Enden sind zur wässrigen Phase ausgerichtet, wodurch sie die Emulsion eine Zeit lang stabilisiert und homogen erscheint. Trotz der enthaltenen natürlichen Emulgatoren rahmt Milch nach einigem Stehen auf. Anschließend kann der Rahm an der Oberfläche abgeschöpft werden, da Fette eine geringere Dichte als Wasser haben. Um dieses Phänomen zu verhindern, wird die Milch homogenisiert, das heißt durch starkes Rühren werden die Fett Tröpfchen besonders fein verteilt.
Wichtige Definitionen
Emulsion
Von einer Emulsion wird gesprochen, wenn mehrere Flüssigkeiten heterogen miteinander gemischt sind.
Suspension
Von einer Suspension wird gesprochen, wenn ein Feststoff in einer Flüssigkeit heterogen vermischt ist.
Dispersion
Von einer Dispersion wird gesprochen, wenn ein heterogenes Gemisch aus einem flüssigen oder festen Stoff in einer Flüssigkeit besteht.
Legierung
Von einer Legierung wird gesprochen, wenn eine homogene Mischung aus mehreren Metallen besteht.
Lösung
Von einer Lösung wird gesprochen, wenn eine homogene Mischung aus einem festen, flüssigen oder gasigen Stoff in einer Flüssigkeit besteht.
Gemenge
Von einem Gemenge wird gesprochen, wenn eine heterogene Mischung aus mehreren Feststoffen besteht.
Aerosol
Von einem Aerosol wird gesprochen, wenn eine Flüssigkeit oder ein Feststoff heterogen in einem Gas vermischt sind.
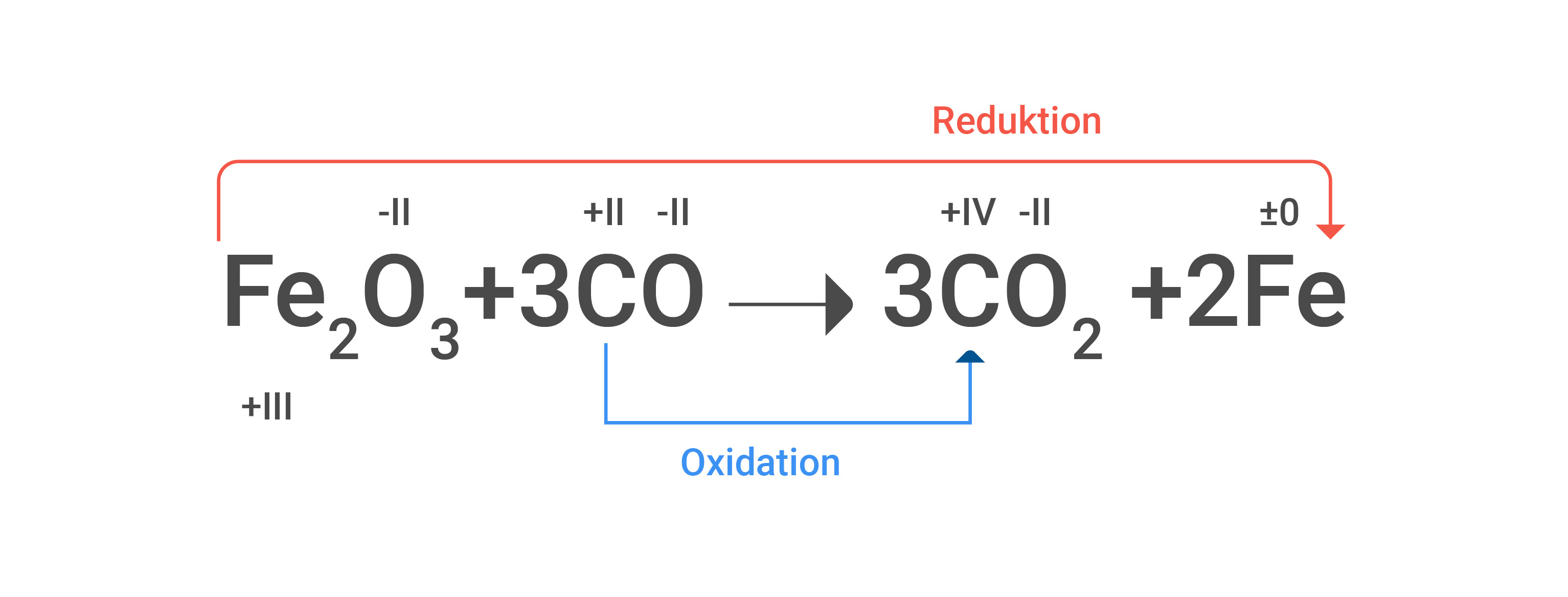
Redoxreaktionen
Eine Redoxreaktion (gesprochen: redóksreaktion; eigentlich: Reduktions-Oxidations-Reaktion) ist eine chemische Reaktion. Bei dieser Reaktion überträgt ein Reaktionspartner Elektronen auf den anderen. Es findet bei einer solchen Elektronenübertragungsreaktion eine Elektronenabgabe (Oxidation) sowie eine Elektronenaufnahme (Reduktion) statt.
Reaktionsablauf
Die Redoxreaktionen laufen immer gleich ab. Ein Stoff A reagiert mit mindestens einem Stoff B. Stoff A ist dabei der Donator und gibt Elektronen ab und Stoff B der Akzeptor, welcher Elektronen aufnimmt.
A → A+ + e-
Das allgemeine Reaktionsschemata lautet
Oxidation
Stoff A gibt ein Elektron ab und ist somit das Reduktionsmittel. Bei einer Oxidation handelt es sich um eine chemische Reaktion, bei der ein Atom, Ion oder Molekül Elektronen abgibt. Dabei nimmt ein anderer Stoff die Elektronen auf und wird dadurch reduziert.
B + e- → B-
Reduktion
Das Elektron wird vom Oxidationsmittel B aufgenommen. Bei einer Reduktion handelt es sich um eine chemische Reaktion, bei der Elektronen von einem Atom, Ion oder ein Molekül aufgenommen werden. (Tipp: Bei einer Reduktion wird die Oxidationszahl reduziert). Sie tritt zusammen mit der Oxidation auf, welche der gegenteilige Fall der Reduktion ist. Beide Phänomene laufen nie unabhängig voneinander ab. Zusammen werden sie als Redoxreaktion bezeichnet.
A + B → A+ + B-
Redoxreaktion
Stoff A gibt ein Elektron an Stoff B ab. Um herauszufinden, welcher Stoff in einer Reaktion oxidiert oder reduziert wird, kann die formale Oxidationszahl angewandt werden.
Spezialfälle der Redoxreaktionen
Komproportionierung
Hier reagiert eine gleiche Atomsorte mit je einer hohen und einer niedrigeren Oxidationszahl zu einem Produkt mit mittlerer Oxidationszahl. Bei diesem Spezialfall handelt es sich also um eine gleichzeitige Reduktion und Oxidation eines Atoms aus einer höheren und einer niedrigeren Oxidationsstufe. Dabei bildet sich eine dazwischen liegende Oxidationsstufe.
Bekannte Komproportionierungen: Reaktion von Iodid mit Iodat Hierbei wird Iodid durch Iodat zu Iod oxidiert und das Iodat selbst wird zu Iodid reduziert.
Oder: die Entladung eines Bleiakkumulator (Autobatterie). Hierbei reagieren Blei und Blei(IV)oxid zu Bleisulfat unter der Wirkung von Schwefelsäure.
IO3 - + 5l- + 6H3O+ → 3I2 + 9H2O
Iod geht von Oxidationsstufen +IV (Iodat) und -I (Iodid) auf 0 (Iod)
Pb + PbO2 + H2SO4 → 2PbSO4 + 2H2O
Blei geht von Oxidationsstufen +IV und 0 auf +II
Disproportionierung
Die Disproportionierung ist auch ein Spezialfall einer Redoxreaktion. Es ist das Gegenteil einer Komproportionierung. Bekannte Disproportionierungsreaktionen sind beispielsweise die Aufladung eines Bleiakkumulators (Autobatterie). Hierbei reagiert Bleisulfat zu Blei(IV)oxid und Blei.
2PbSO4 + 2H2O → + PbO2 + H2SO4
Blei geht von Oxidationsstufe +II zu 0 und +IV
Reaktionsgleichung
In der Chemie ist eine Reaktionsgleichung die Kurzschreibweise für eine chemische Reaktion. Die Reaktionsgleichung gibt die Edukte und Produkte einer Stoffumwandlung in Formelschreibweise wieder. Wichtig hier ist, dass diese Formelschreibweise international einheitlich ist. Die Edukte und Produkte sind jedoch bei einer Stoffumwandlung nicht gleich. Daher wird aus didaktischen Gründen oft die Bezeichnung “Reaktionsschema” benutzt.
Grundsätzlicher Aufbau eines Reaktionsschemas
In einem Reaktionsschema befinden sich links vom Reaktionspfeil die Ausgangsstoffe der Stoffumwandlung. Rechts vom Reaktionspfeil befinden sich die Endstoffe der Stoffumwandlung. Die beteiligten Stoffe werden dabei als Summenformeln oder als Strukturformeln wiedergegeben.
Beispiel: Gemisch aus Eisen- und Schwefelpulver reagiert nach Zündung zu Eisen(II)-sulfid.
In Worten lautet das Reaktionsschema:
Eisen + Schwefel → Eisen (II )- Sulfid
Symbole der Elemente:
Fe + S → FeS
Bestandteile und Symbole im Reaktionsschema
Zusätzlich zu den bereits genannten Bestandteilen finden sich in einem Reaktionsschema in Formelschreibweise groß geschriebene Zahlen zur Wiedergabe von Stoffmengen-Verhältnissen. Ebenso gibt es etwaige Angaben über die Aggregatzustände der beteiligten Stoffe ((g) für gasförmig, (l) für flüssig, (s) für fest und (aq) für in wässriger Lösung) oder elektrische Ladungen der Teilchen, der Ionen. Zuletzt gibt es noch einen Pfeil nach oben hinter einer Formel oder einen Pfeil nach unten. Der Pfeil nach oben zeigt das Entweichen eines Gases aus einer Flüssigkeit oder einem Feststoff an (↑). Der Pfeil nach unten zeigt den Niederschlag eines unlöslichen Feststoffes aus einem flüssigen oder gasförmigen Reaktionsgemisch an (↓).
Der Reaktionspfeil als Bestandteil des Reaktionsschemas
Der Reaktionspfeil symbolisiert die chemische Reaktion. Er wird als ➝ geschrieben, bei umkehrbaren Reaktionen auch als ⇌. Dieser Pfeil wird auch als Gleichgewichtspfeil bezeichnet.
Arten chemischer Reaktionen
Es gibt vier grundlegenden Möglichkeiten einer Stoffumwandlung (auch chemische Reaktion genannt):
Stoffumgruppierung
A → B
Stoffzerlegung
A → B + C
Stoffvereinigung
A + B → C
Stoffumgruppierung in Form von Austauschreaktion – Synthese mit Analyse in Kombination
A + B → C + D sowie A + BC → A + BC → AB + C
Du willst deine Noten an der Uni verbessern und suchst die perfekten Lernunterlagen für deinen Studiengang? Dann schau doch mal auf Studydrive vorbei.
Hier findest du viele, viele kostenlose Lernunterlagen, Übungsblätter, Altklausur-Lösungen und kannst dich mit anderen Studis austauschen.