Die besten Organische Chemie Zusammenfassungen

Zusammenfassung.pdf

Organische Chemie Zusammenfassung.pdf

Wichtig Begriffe Organische Chemie.docx

Organische Chemie Zusammenfassung.pdf

Organische Chemie .pdf

Chemie Zusammenfassung.doc


Das Fachgebiet Chemie setzt sich aus verschiedenen Teilbereichen zusammen. Zu diesen zählen die Anorganische, die Organische, die Physikalische und die Analytische Chemie. Die Organische Chemie gilt als der umfangreichste Teilbereich.
Chemie bzw. chemische Anwendungen sind bereits in der Antike bekannt gewesen. Trotzdem dauerte es bis ins 18. Jhd., bis eine Trennung in die Teilbereiche organische und anorganische Chemie erfolgte. Diese Trennung geht auf den schwedischen Mediziner und Chemiker Jöns Jakob Berzelius zurück. Er gilt als Vater der modernen Chemie. Berzelius teilte die Stoffe in belebte und unbelebte, also in organische und anorganische, Stoffe ein. Die Trennung von Stoffen beruhte in der Annahme, dass eine Lebenskraft erforderlich sei, um organische Stoffe zu bilden. Der Chemiker Wöhler zeigte 1828, dass beim Erhitzen von Ammoniumcyanat (anorganische Verbindung), Harnstoff (organische Verbindung) entsteht. Somit konnte die Annahme von Berzelius im 19. Jahrhundert widerlegt werden.
Die Definition des Begriffs “Organische Chemie”, so wie wir ihn auch heute noch kennen, lässt sich auf den französischen Chemiker und Naturwissenschaftler Antoine Laurent de Lavoisier zurückführen. Dieser erkannte in seinen Untersuchungen, dass alle organischen Verbindungen Kohlenstoff enthalten. Dies ist der Grund, warum wir heute unter der Organischen Chemie die “Chemie der Kohlenstoffverbindungen” verstehen.
Wie bereits erwähnt, geht die Definition der Organischen Chemie auf Lavoisier zurück. Trotz dessen gibt es keine streng gültigen Unterscheidungsmerkmale zwischen den organischen und den anorganischen Verbindungen. Ein Grund dafür ist zum Beispiel, dass es Kohlenstoffverbindungen gibt, die ebenfalls zur Anorganischen Chemie gezählt werden (z.B. CO2 und alle Derivate, HCN und alle Derivate). Hinzu kommt, dass folgende Aussage nicht immer zutrifft: “[...] in anorganischen Verbindungen sind die Atome durch Ionenbindungen und in organischen Verbindungen durch Atombindungen miteinander verknüpft.” Trotz der generell zutreffenden Aussage, organische Verbindungen seien, im Gegensatz zu anorganischen Verbindungen, brennbar, lässt sich daraus keine streng gültige Regel ableiten.
In der Chemie werden alle Verbindungen durch eine bestimmte “Formelschreibweise” wiedergegeben. Diese Formelschreibweisen sind abhängig davon, welcher Aspekt mit Hilfe der Formel wiedergeben werden soll. Die am häufigsten verwendeten Formeln, zur Wiedergabe von Stoffen, sind die Summenformel, Verhältnisformel, Valenzstrichformel und die Strukturformel.
Die einfachste Wiedergabe von organischen Kohlenwasserstoff-Verbindungen erfolgt durch die sogenannte Strichformel. Sie wird auch als Skelettformel bezeichnet. Bei dieser Struktur werden alle H-Atome weggelassen und nur die C-C-Bindungen als Striche dargestellt. Sind jedoch noch andere Atome in der Verbindung enthalten, so werden diese eingezeichnet. Damit es für andere und natürlich auch für einen selbst verständlicher ist und um die räumliche Struktur der Verbindung anzudeuten, werden die Bindungen (bei Einfachbindungen) in Zick-Zack-Form wiedergegeben.
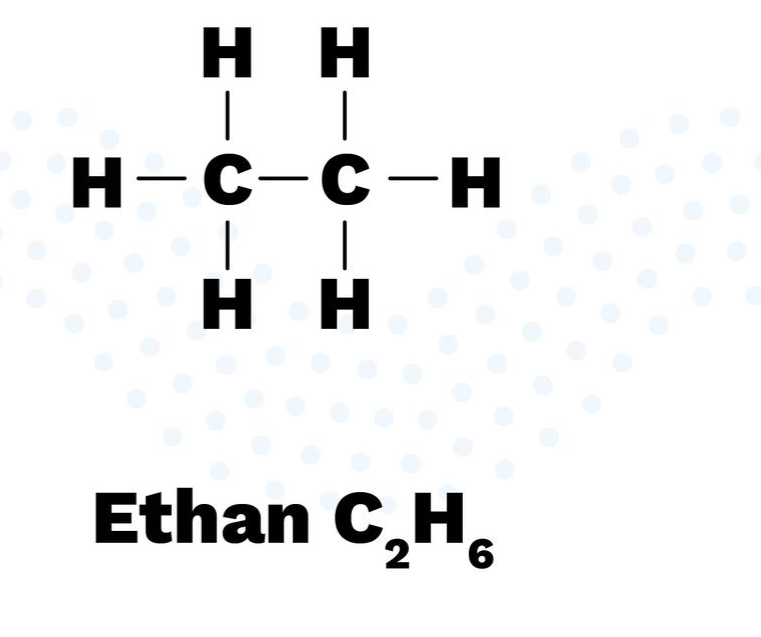
Die Lewisformel ist die, im Anfangsunterricht der Organischen Chemie, am meisten verwendete Darstellungsform von Strukturen. Bei dieser Schreibweise wird ausgenutzt, dass das Reaktionsverhalten von Atomen von der Zahl der Außenelektronen bestimmt wird. Daher werden bei einem Atom nur die entsprechenden Außenelektronen bzw. Bindungselektronen angegeben. Diese werden dabei durch Punkte bzw. Striche um das Elementsymbol dargestellt. Punkte stellen dabei die Elektronen dar und Striche die Elektronenpaare.
Kohlenstoff unter allen Elementen, nimmt eine einzigartige Stellung ein. Denn Kohlenstoff hat nach seiner Stellung im Periodensystem wenig Neigung, Ionenbindungen einzugehen. Dies liegt an dessen Elektronegativität, die mit 2,5 eher in der Mitte der Skala liegt. Für eine Ionenbindung wird eine Elektronegativitätsdifferenz von 1,7 benötigt. Kohlenwasserstoffe enthalten sowohl C-Atome als auch H-Atome und bilden Atombindungen. Die niedrige Elektronegativitätsdifferenz von C-H Bindungen sorgt dafür, dass das Kohlenstoffatom gering polarisiert ist. Somit wird der Angriff von polaren Reaktionspartnern erschwert. Daher ermöglicht es eine Ausbildung einer Vielfalt von kettenförmigen und ringförmigen Verbindungen zu bilden. Somit sind Kohlenstoffverbindungen eine einzigartige Stoffklasse.
Es gibt mehrere hunderttausend anorganische Verbindungen und mehrere Millionen organische Verbindungen. Der Grund dafür ist die Sonderstellung des Kohlenstoffs: Das Kohlenstoffatom verfügt über 4 Valenzelektronen. Um die Edelgaskonfiguration zu erreichen, kann das Kohlenstoffatom vier Atombindungen mit anderen Bindungspartner eingehen. Neben der Einfachbindung kann das Kohlenstoffatom auch Doppelbindung oder Dreifachbindung ausbilden. Nur durch die Ausbildung von unterschiedlichen Mehrfachbindungen kann eine Vielzahl von verschiedenen Strukturmöglichkeiten erzielt werden, die es in der anorganischen Chemie kaum gibt. Dazu kommt der Fakt, dass ein Kohlenstoffatom bis zu vier Bindungen zu anderen Bindungspartnern ausbilden kann. Dies ermöglicht eine Vielzahl von unterschiedlichen dreidimensionalen Strukturen. Daher sind neben linearen oder verzweigten Kohlenstoffketten auch Kohlenstoffringe oder Netzwerke aus Kohlenstoffatomen möglich.
Es gibt viele organische Verbindungen, die aus einem Kohlenstoffwasserstoff-Gerüst aufgebaut werden. Anhand von herangezogenen Bindungstheorien würde sich zeigen lassen, dass die Ladungsverteilung der Bindungselektronen zwischen dem Kohlenstoff- und dem Wasserstoffatom fast symmetrisch ist. Dies bedeutet, dass die Elektronegativitätsdifferenz der Bindung relativ klein ist. Somit handelt es sich bei einer C-H-Bindung um eine schwach polare Atombindung. Wie bereits erwähnt, sind polare Bindungen in der Regel reaktiver als unpolare und schwach polare Bindungen. Der Grund dafür ist, dass der elektronegativere Bindungspartner die Bindungselektronen stärker an sich zieht und somit die Bindung gelockert wird. Daher wird bei der C-C- oder C-H-Einfach-Bindungen im Vergleich zu anderen Bindungen eine große Aktivierungsenergie benötigt, um solche “Stoffe” zur Reaktion zu bringen, wie zum Beispiel, um neue Bindungen auszubilden. C-H bzw. C-C-Einfachbindungen werden daher auch als chemisch inert bezeichnet, was bedeutet, dass sie wenig reaktionsfreudig sind.
Der Elektronegativitätswert des Kohlenstoffatoms liegt bei 2,5 und somit etwa in der Mitte der Skala. Daher zeigt das Kohlenstoffatom auch in etwa gleich starke Tendenz, Elektronen aufnehmen als auch Elektronen abzugeben. Daher kann das Kohlenstoffatom mit elektronegativen, als auch elektropositiven Elementen eine Bindung ausbilden. Der Grund hierfür liegt daran, dass das Kohlenstoffatom mit 4 Valenzelektronen eine halb-besetzte Valenzschale besitzt. Um eine vollbesetzte Valenzschale zu erhalten, hat das Kohlenstoffatom die Wahl zwischen vier Valenzelektronen abgeben oder vier Elektronen aufnehmen. Betrachtet wir hierzu die Anorganische Chemie, zeigt sich, dass alle Elemente eine bestimmte Neigung dazu haben, die Edelgaskonfiguration zu erreichen. Dies bedeutet, dass die Elemente eine volle Valenzschale erreichen wollen. Metalle haben die Tendenz dazu, lieber Elektronen abzugeben. Doch anstelle dessen, dass bei Nichtmetallen der Gegensatz der Falls ist, haben Nichtmetalle nicht die Tendenz dazu, lieber Elektronen aufzunehmen. Diese besonderen Eigenschaften des Kohlenstoffatoms erklären dessen Sonderstellung sowie die Vielfalt der organischen Stoffe, welche es im Vergleich zu den anorganischen Stoffen gibt.
Wie bereits erwähnt wurde, ergibt sich aufgrund der Sonderstellung des Kohlenstoffatoms eine große Vielfalt organischer Verbindungen. Daher ist es essenziell die organischen Verbindungen im ersten Schritt grob in Stoffklassen zu unterteilen.
Organische Verbindungen teilt man als Erstes nach dem Aufbau des Kohlenstoffgerüsts ein. Hier gibt es eine Unterscheidung zwischen kettenförmigen und ringförmigen Kohlenstoffgerüsten. Die Kettenförmigen werden auch azyklisch und die Ringförmigen zyklisch genannt. Der Begriff “azyklisch” sollte jedoch nicht mit dem Begriff “aliphatisch” vermischt werden. Aliphatische organische Verbindungen sind verzweigte oder unverzweigte, ketten oder ringförmige Kohlenwasserstoffketten. Sie verfügen über keine “aromatische” Struktur. Daher sind alle organischen Verbindungen, die nicht aromatisch sind, aliphatisch. Liegen kettenförmigen Verbindungen vor, gibt es eine weitere Unterscheidung in gesättigte und ungesättigte Kohlenwasserstoffe. Wenn alle Kohlenstoffatome in der Verbindung nur über Einfachbindungen gebunden sind, liegt ein gesättigter Kohlenwasserstoff vor. Wenn jedoch C-C-Mehrfachbindungen vorliegen, wird von ungesättigten Kohlenwasserstoffen gesprochen. Kohlenwasserstoff-Verbindungen können aliphatisch oder aromatisch sein, wenn sie ringförmig dar liegen. Aliphatische, ringförmige Verbindungen werden alicyclisch genannt.
Ebenso gibt es Verbindungen, die als Heterozyklus bezeichnet werden. Diese liegen vor, wenn eine ringförmige Verbindung besteht, in dessen Struktur ein anderes Element als Kohlenstoff an der Ringbildung beteiligt ist.
Auf Studydrive findest du jede Menge Lernmaterialien, die dir bei der Kurs- oder Prüfungsvorbereitung helfen werden. Hier findest du Zusammenfassungen und Notizen, Lösungen zu vergangenen Prüfungen und Arbeitsblätter.











Mit unserem smarten Karteikarten-Tool kannst du dein Wissen schnell und effektiv testen oder easy von unterwegs lernen. Erstelle einfach deine eigenen Karteikarten oder übe mit denen deiner Kommilitonen.
Melde dich jetzt bei Studydrive an und erhalte kostenlos Zugang zu allen Kursen, die zu deinem Thema passen. Tausche dich außerdem mit anderen Studierenden aus und bekomme hilfreiche Antworten auf all deine Fragen!