Atommasse und Radioaktivität

Inhaltsübersicht
Massendefekt, Kernzerfall, Molare Masse und das Mol
Wie wir wissen, besteht ein Atom aus drei Elementarteilchen – dem Proton, Neutron und Elektron. Protonen und Neutronen befinden sich im Kern eines Atoms. Daher werden sie zusammen als Nukleonen (lat. nucleus „Kern“) bezeichnet. Doch alle drei Elementarteilchen sind für die Berechnung der Atommasse notwendig. Wenn die Masse einzelner Elemente abnehmen, so liegt es daran, dass sie zerfallen und somit radioaktiv sind.
Atommasse und Massendefekt
Die Atommasse setzt sich aus Protonen, Neutronen und Elektronen zusammen. Die Masse eines Nuklids (Link Isotope) ist allerdings stets kleiner als die Summe der Massen seiner Bausteine (also der Elementarteilchen). Man nennt dies den Massendefekt. Dieser kann mit dem Einsteinschen Gesetz der Äquivalenz von Masse und Energie E = m · c2 verstanden werden. Demnach ist also Masse in Energie umwandelbar und umgekehrt. Bei der Vereinigung von Protonen und Neutronen zu einem Kern wird die Kernbindungsenergie aufgebracht und reduziert folglich die Masse. Die Energieabnahme des Kerns ist äquivalent der Massenabnahme.
Folglich, wie im Rechenbeispiel gezeigt, wiegt das 42He-Atom weniger als die Summe seiner Teilchen. Der Grund ist die Äquivalenz von Masse und Energie. Die benötigte Energie für die Kernbindung wird durch die Masse gewonnen bzw. die fehlende Masse wurde in die Kernbindungsenergie umgewandelt, die die Elementarteilchen zusammenhält. Bei Kernreaktionen gilt die Massenhaltung nicht, bei chemischen Reaktionen hingegen schon, weil die Bindungsenergien wesentlich kleiner sind.
Mehr über das Atom und seine Elementarteilchen findest du übrigens hier.
Kernzerfall und Radioaktivität
Bei Kernzerfall und Radioaktivität spielen nur die Kernteilchen eine Rolle, die Elektronenhülle ist nicht relevant. Denn Elemente können in andere Elemente zerfallen und hierbei entscheidet der Kern, um welches Element es sich handelt. Es gibt verschiedene Prozesse, wie ein Element sich in ein anderes umwandelt. Dabei kann dieser Prozess allgemein folgend definiert werden, wobei E hier ein radioaktives Element darstellt:
A zE → A‘ Z’E‘ + A”Z”E”
Folgend muss immer gelten: A = A‘ + A“ und Z = Z‘ + Z“, wenn keine weiteren Teilchen entstehen. Die Halbwertzeit τ1/2 definiert, die Zeit, nach der die Hälfte der radioaktiven Kerne zerfallen sind. Die Zerfälle werden in verschiedene Klassen eingeteilt.
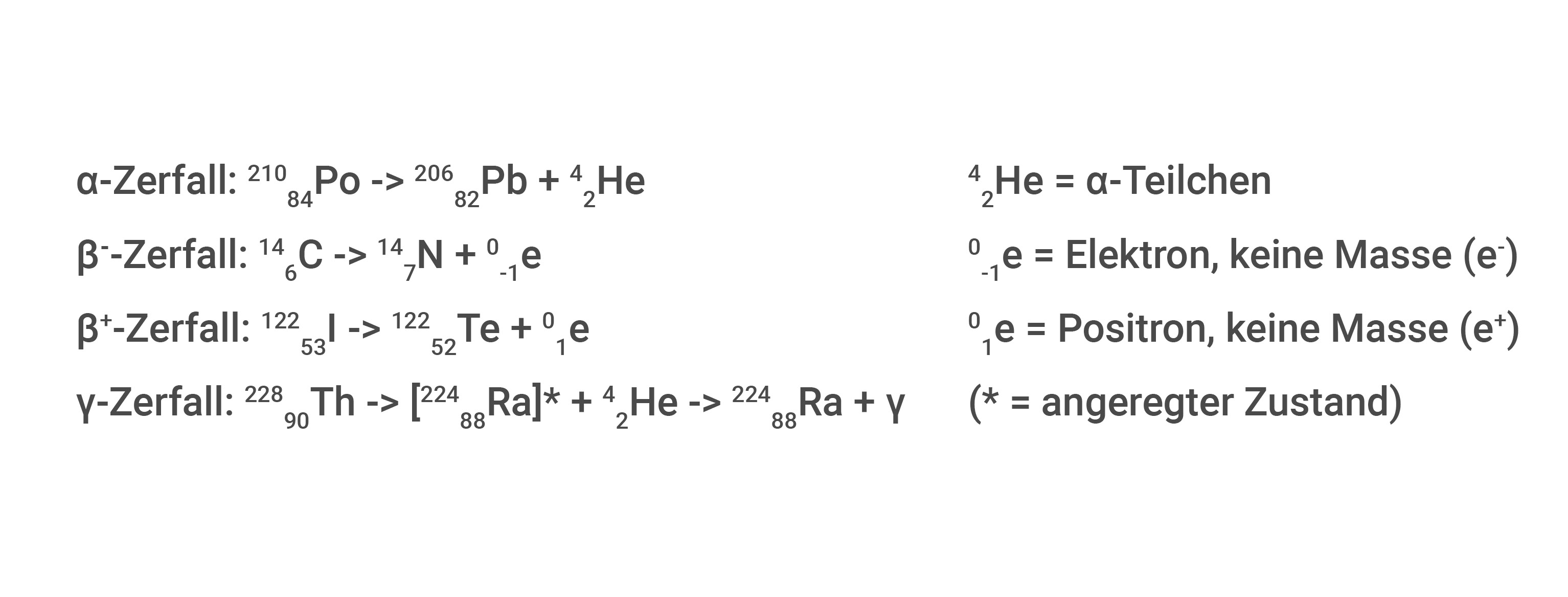
Altersbestimmung mit dem 14 6C-Isotop
Kohlenstoff kommt in der Natur in Form mehrerer Isotope vor: 12 6C, 13 6C, 14 6C. Das 146C ist radioaktiv und hat eine Halbwertzeit von t1/2 = 5730 Jahren. Es entsteht z.B. durch Wechselwirkungen von CO2 in der oberen Atmosphäre mit kosmischer Strahlung. Das entstandene radioaktive CO2 kann durch den Austausch von Atmosphärenschichten in die erdnahe Schicht gelangen. Die Konzentration von radioaktivem CO2 in der Atmosphäre ist durch diesen Austausch immer konstant. Es wird von Pflanzen aufgenommen und mittels der Photosynthese in Kohlenhydrate umgewandelt. Auch Tiere nehmen mit der Nahrung (den Pflanzen) dieses radioaktive CO2 auf. So enthalten alle Lebewesen einen konstanten Anteil 14 6C. Sobald ein Lebewesen stirbt, kann es jedoch mit seiner Nahrung kein weiteres 14 6C mehr aufnehmen. Der vormals konstante 146C-Gehalt sinkt nun kontinuierlich mit dem radioaktiven Zerfall. Der 14 6C-Gehalt kann später nach dem Tod des Lebewesens mittels der Massenspektrometrie bestimmt werden. Die bekannte Halbwertzeit des 14 6C ermöglicht es, den Zeitpunkt des Todes (Ausbleiben der Photosynthese) zu bestimmen.
Relative Atommasse Ar („Atomgewicht“)
Ein Atom hat eine sehr geringe Masse. Würde man diese relative Atommasse Ar eines Heliumatoms in der uns vertrauten Masseneinheit kg angeben, so wäre die sich ergebende Zahl sehr klein und daher schlecht zu handhaben: m (42He) = 6,6465 · 10-27 kg
Daher gibt man die Atommassen relativ zu einer ähnlich großen Masse an:
1 u = Atommasseneinheit.

Das Mol n (Stoffmenge)
Möchte man eine Stoffmenge angeben, so bedient man sich häufig der Teilchenanzahl. In der Chemie bestehen die betrachteten Stoffmengen jedoch aus einer sehr großen Teilchenzahl. Da diese Zahlen sehr unhandlich sind, hat man das Mol eingeführt. Eine Stoffmenge n, die aus 6,022·1023 Teilchen besteht, nennt man ein Mol. Die Einheit ist „mol“ (SI-Einheit!). Ein Mol ist festgelegt als die Stoffmenge, die exakt so viele Teilchen enthält, wie Atome in 12 g 12 6C enthalten sind. 6,022·1023 = Avogadro-Konstante (NA) = Lohschmidt-Konstante (NL) 6,022·1023 Teilchen 12 6C wiegen exakt 12 g oder 12 g 12 6C enthalten NA Teilchen.
| mikroskopisch | Einheit | makroskopisch |
|---|---|---|
| U | Masse | Kg |
| Teilchenzahl | Anzahl | Mol |
| eV | Energie | J |
Die molare Masse M
Die molare Masse gibt das Gewicht eines Mols eines bestimmten Elements an. Sie entspricht also dem, was 6,022·1023 Teilchen dieses Elements wiegen.
1 Teilchen des Kohlenstoffnuklids 12 6C wiegt 12 u → 1 mol 12 6C wiegen 12 g:
M (126C) = 12 g/mol = 12·10 -3 kg/mol
Im PSE ist jedoch für Kohlenstoff nicht 12 g/mol, sondern M = 12,011 g/mol angegeben. Dies liegt daran, dass das Element Kohlenstoff in Form von 3 verschiedenen Isotopen vorkommt:
12 6C (98,9%), 136C (1,1%), 146C (Spuren)
Der im PSE angegebene Wert bezieht sich also auf das natürliche Gemisch der Isotope.
Rechenbeispiel: Welche molare Masse hat Kohlenstoff, wenn es zu 98,9% aus 12 C und zu 1,1% aus 13 C besteht?
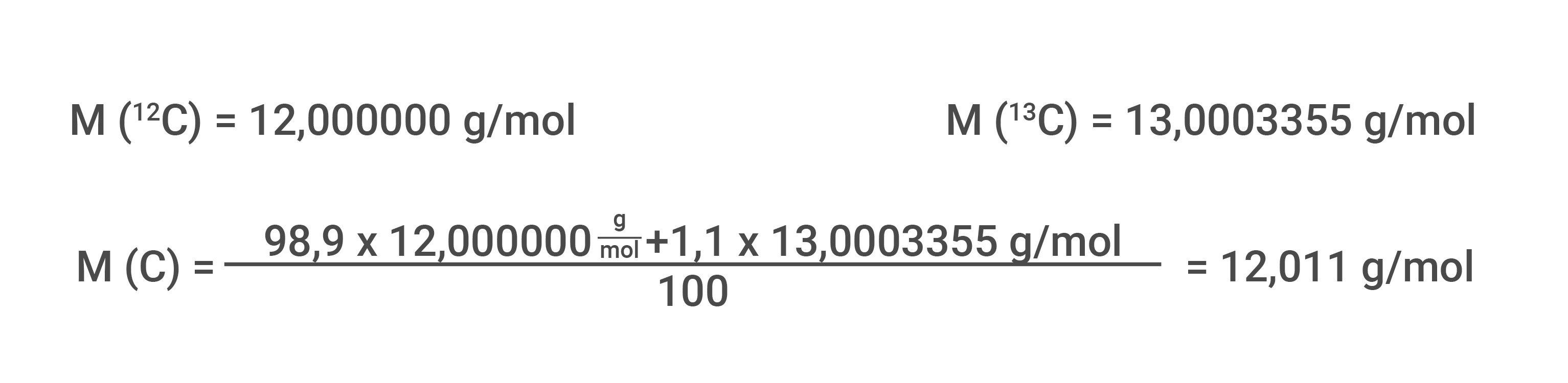
Elementarer Sauerstoff besteht zu einem sehr großen Teil aus 16O: M(O) = 15,999 g/mol. Chlor dagegen kommt hauptsächlich in zwei Isotopen vor: M(Cl) = 35,453 g/mol. Die molare Masse M lässt sich nicht nur von Elementen ermitteln, sondern man kann auch die molare Masse von Verbindungen errechnen.

