Die besten Zusammenfassungen

Periodensystem .pdf

Atome & Periodensystem .pdf


Das Periodensystem ist heute das wichtigste Werkzeug eines Chemikers. Nur mit Hilfe dieser besonderen Tabelle lassen sich bestimmte Trends und Eigenschaften erkennen. Ebenso können viele chemische Reaktionen mit ihr erklärt oder sogar vorhergesagt werden.
Das Periodensystem der Elemente dient als Organisationsschema und wurde erstmals von Dmitri Mendelejew und Lothar Meyer (unabhängig voneinander, allerdings zufällig zur etwa gleichen Zeit – 1869 – und sehr ähnlich) schematisch dargestellt. Im Laufe der Zeit konnten mithilfe des Periodensystems unentdeckte Elemente vorhergesagt werden, da es einem besonderen Schema folgt. Ebenfalls wurden einige Eigenschaften nun erstmals deutlich und vorhersehbar, da sich diese in einer bestimmten Reihe von Elementen wiederholt haben und somit auch auf die weiteren Elemente angewandt werden konnten.
Man kennt das klassische Periodensystem der Elemente aus der Schule. Es ist eine Tabelle, in der die Elemente nach einfachen Regeln geordnet sind. Die chemischen Elemente werden nacheinander ihrer Anzahl der Protonen nach im Atomkern angeordnet.
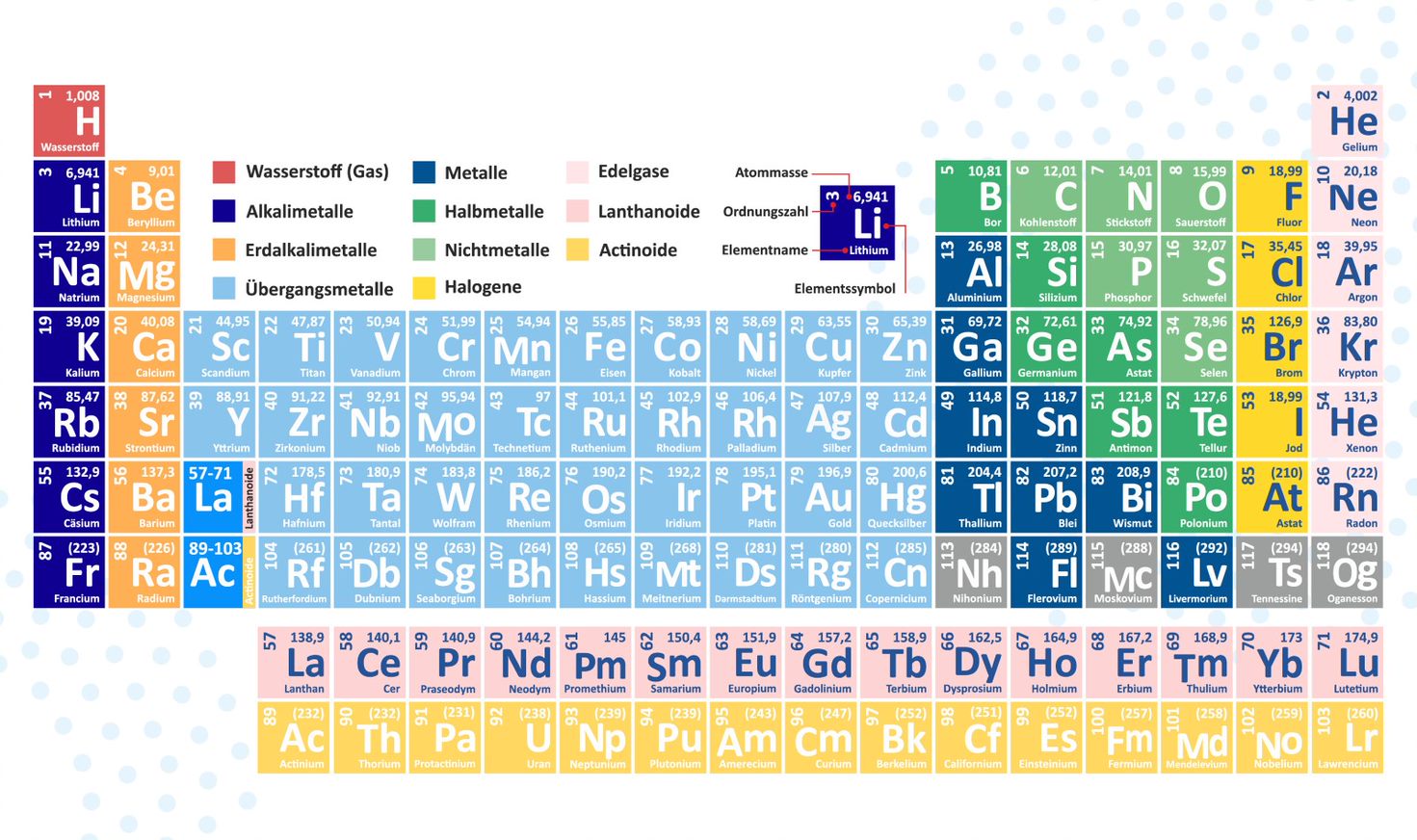
Diese Zahl drückt sich in der Ordnungszahl aus. Gleichzeitig gibt diese Zahl die Anzahl der Elektronen an. Das liegt daran, da die Elemente neutral sein müssen und sich die Positivität der Protonen und die Negativität der Elektronen sich mit gleicher Zahl ausgleichen können.
Mit steigender Ordnungszahl von links nach rechts stehen die Elemente also hintereinander in einer „Zeile“. Die Reihenfolge ist somit geklärt. Wann es zur nächsten Zeile, die sogenannte Periode, kommt, verrät ebenso die Ordnungszahl. Allerdings ist dies schwerer nachzuvollziehen. Daher kann man sich den Atomaufbau näher anschauen, um zu verstehen, wann es zur nächsten Periode kommt.
Wichtig dabei ist zu erwähnen, dass sich bestimmte Eigenschaften mit wachsender Ordnungszahl wiederholen. Dadurch hat man sich für den Begriff „Periode“ entschieden und das Ganze schließlich „Periodensystem“ genannt.
Beim Atomaufbau wird die Vorstellung eines Atoms mit einem Schalenmodell verknüpft. Hierbei gilt es zu beachten, dass der Atomkern bestehend aus Protonen und Neutronen von Schalen umgeben ist. Die umliegenden Schalen können als Kreise um den Kern schematisch dargestellt werden.
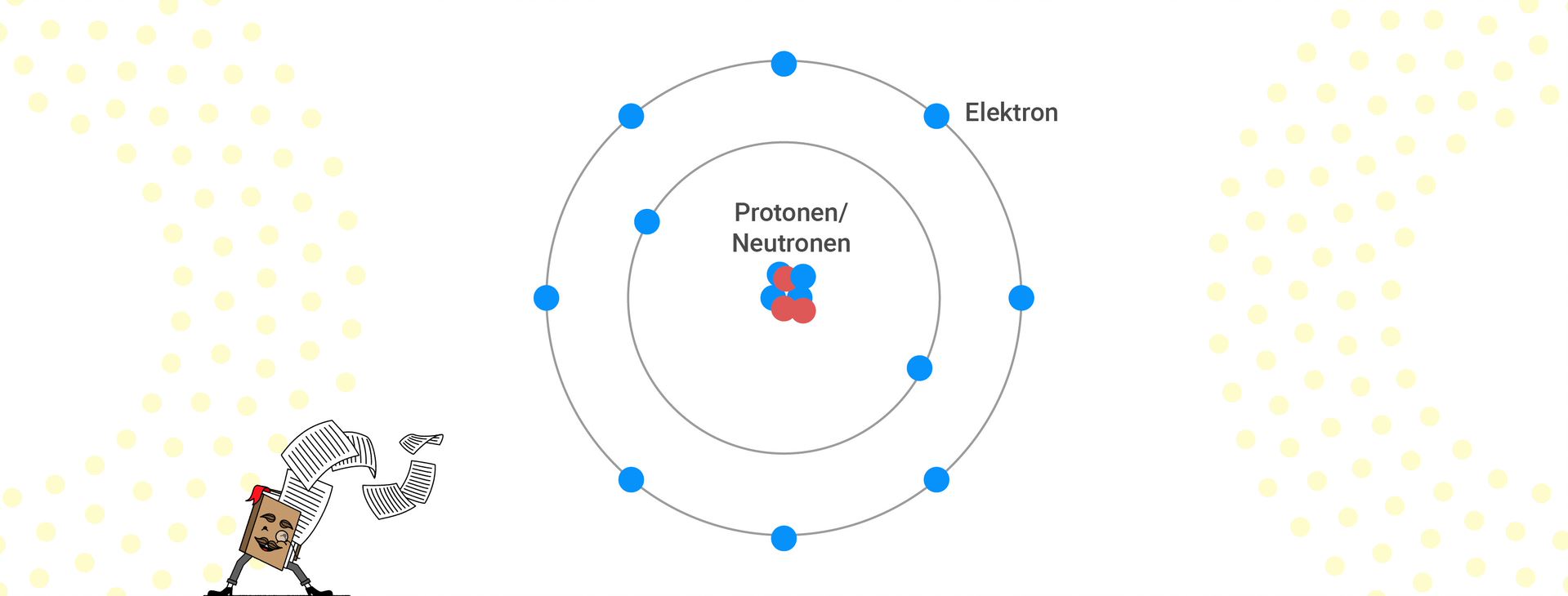
Auf der ersten Schale dürfen sich maximal zwei Elektronen aufhalten. Die erste Schale stellt somit die erste Periode dar, in der sich Wasserstoff und Helium befinden. In der zweiten Schale dürfen sich nun acht Elektronen gleichzeitig aufhalten. Somit kommen wir zur zweiten Periode. Auch in der dritten und in den nächsten Perioden sind wieder acht Elektronen erlaubt. Faustregel: Die erste Schale besitzt maximal zwei Elektronen, ab der zweiten Schale dürfen sich maximal acht Elektronen aufhalten. Bei jeder neuen Schale folgt eine neue Periode.
Neben den Perioden gibt es auch die sogenannten Gruppen. Die Gruppen stellen die Spalten dar. Dabei ist erkennbar, dass die Elemente mit chemisch ähnlichen Eigenschaften in einer Gruppe stehen. Diese Gruppen werden mit verschiedenen Begriffen beschrieben und unterschieden. Auch kann zwischen Hauptgruppen und Nebengruppen unterschieden werden. Wir beschäftigen uns im Folgenden nur mit den Hauptgruppen.
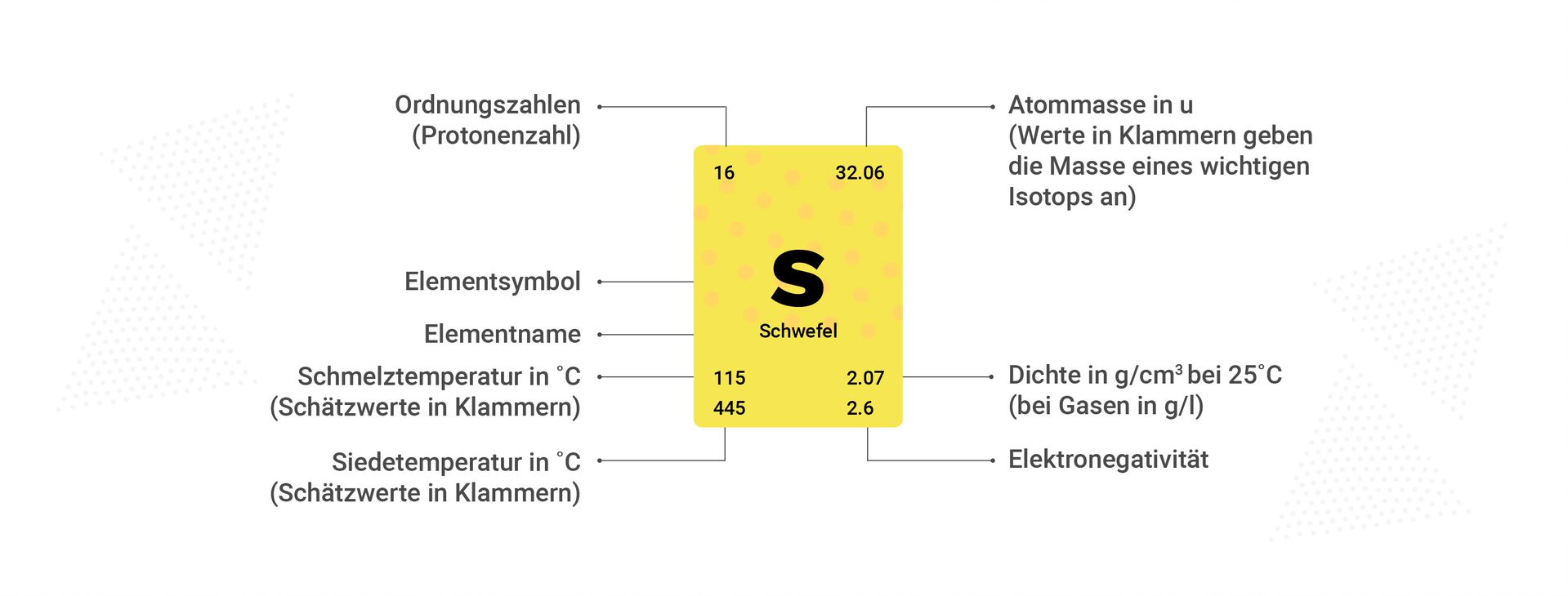
Wie zu Beginn erläutert, gibt das Periodensystem über die Ordnungszahl die Anzahl der Protonen und Elektronen wieder. Das Elementsymbol steht als Abkürzung für das Element. Meist ist auch die Atommasse des Elements im Raster zu finden, welches sich aus der Masse von Protonen, Neutronen und Elektronen berechnen lässt. Die Masse der Elektronen wird allerdings vernachlässigt, wenn man die Anzahl der Neutronen berechnen möchte. Dabei geht man von 1 u für ein Proton bzw. ein Neutron aus.
Bei einer Atommasse von ca. 12 u und 6 Protonen lässt sich die Zahl der Neutronen durch die Differenz berechnen, da die Masse von Protonen 1 u beträgt. Manchmal ist auch die Elektronegativität angegeben, welche ein Maß für die Fähigkeit eines Atoms ist, in einer chemischen Bindung Elektronen an sich zu ziehen. Meist lässt sich auch über die Differenz zweier Elektronennegativitäten von zwei verschiedenen Atomen die Bindung (Link) vorhersagen. Hierbei wird zwischen unpolar, polar und ionisch unterschieden.
Bei farbigen Periodensystemen werden auch über farbliche Kodierungen Eigenschaften deutlich, wie die Zugehörigkeit zu Metallen, Halbmetallen und Nichtmetallen. Außerdem werden über die Perioden die Anzahl der Schalen dargestellt. Ebenso lässt sich über die Nummer der Hauptgruppen die Anzahl der Elektronen in der äußersten Schale vorhersagen. Diese Elektronen tragen einen besonderen Namen, da diese Reaktionen eingehen - sie heißen Valenzelektronen.
Auf Studydrive findest du jede Menge Lernmaterialien, die dir bei der Kurs- oder Prüfungsvorbereitung helfen werden. Hier findest du Zusammenfassungen und Notizen, Lösungen zu vergangenen Prüfungen und Arbeitsblätter.






Melde dich jetzt bei Studydrive an und erhalte kostenlos Zugang zu allen Kursen, die zu deinem Thema passen. Tausche dich außerdem mit anderen Studierenden aus und bekomme hilfreiche Antworten auf all deine Fragen!